热搜词:宏基因组测序 芯片检测

发布时间:2019-03-12 10:00:00 点击数:次

今天给大家分享一篇我们合作客户的高分文章。南方医科大学基础医学院的陈鹏教授在肝病领域权威杂志《Hepatology》上发表佳作,深入探讨了肠道菌群在脓毒症致肝损伤中的调节作用及其机制。

脓毒症(sepsis)是重症监护病房常见病例之一,每年有150万人患脓毒症,该病死率为20%-30%,多器官功能障碍是危重患者死亡的主要原因,脓毒症导致肝损伤是多器官功能障碍的表现之一。肠道菌群及其代谢物一直被认为是肝脏疾病发展的重要介质,然而,肠道菌群在调节脓毒症引起的肝损伤中的调控机制尚不明确。
1)本研究对C57BL/6小鼠采用盲肠结扎穿孔术(CLP)诱发脓毒症及相关肝损伤模型,定义CLP后24小时前后出现垂死症状的小鼠为脓毒症-敏感组,能存活至CLP后七天的小鼠为脓毒症-抵抗组(图1)。
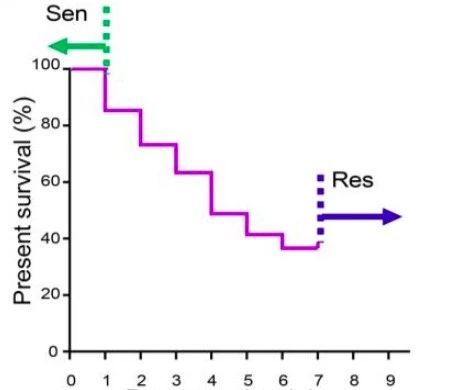
图1敏感鼠和抗性鼠的存活率
2)通过组织学分析,显示敏感组小鼠器官损伤程度和细胞凋亡都比抵抗组更严重;血浆生化参数如ALT,AST和肌酐以及炎症介质水平也证实敏感组小鼠的炎症程度会更高(图2)。
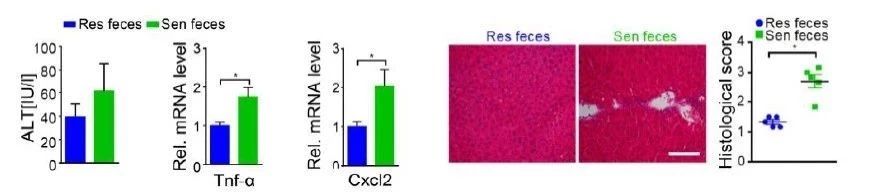
图2敏感鼠和抗性鼠组织水平上特点
3)通过比较敏感鼠和抗性鼠在代谢物水平上的差异,发现两组小鼠的肠道微生物代谢谱也不同。抵抗组小鼠肠道微生物能产生更多的格拉司琼(GA),并且能释放到循环系统中,GA对CLP引起的肝损伤有保护作用,并能显著延长CLP后生存时间。此外,在GA的处理下,LPS诱导巨噬细胞产生促炎症细胞因子(Tnf-α,ll-6)的表达会显著降低。(图3)
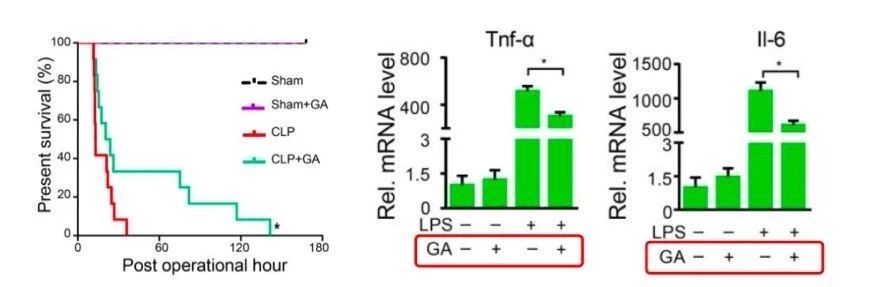
图3 GA对脓毒症引起的肝损伤有保护作用
4)经GA给药的小鼠和经5‐HT3A受体基因敲除的小鼠体内巨噬细胞NF-кB转录激活和p-p38的激活通路均被抑制。肠道微生物产生GA的水平与脓毒症患者血浆ALT/AST水平(肝损伤程度)呈显著负相关(图4B)。
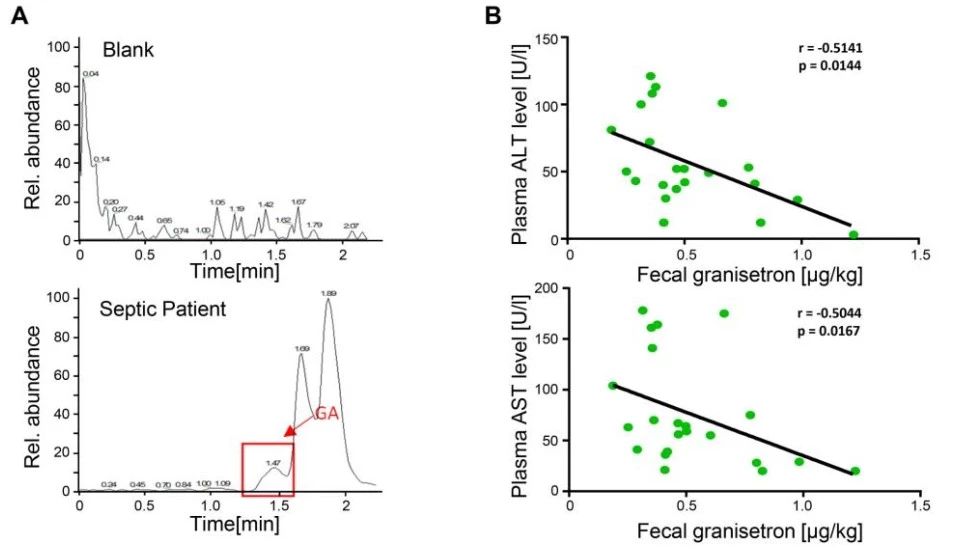
图4A LC-MS检测脓毒症患者和空白对照者粪便中GA量的变化; B 脓毒症患者粪便中的GA和血浆中的ALT/AST相关性分析
5)肠道微生物在该过程中可能起着重要做用,为了进一步验证推论,研究者对小鼠进行了FMT试验,用抗生素处理小鼠五天,进行肠道准备后,再分别移植抵抗组和敏感组小鼠的肠道菌群,考察移植小鼠CLP术后的器官损伤程度(图5)。结果显示,移植了敏感组菌群的小鼠比移植了抵抗组菌群的小鼠表现出了更严重的肝损伤。
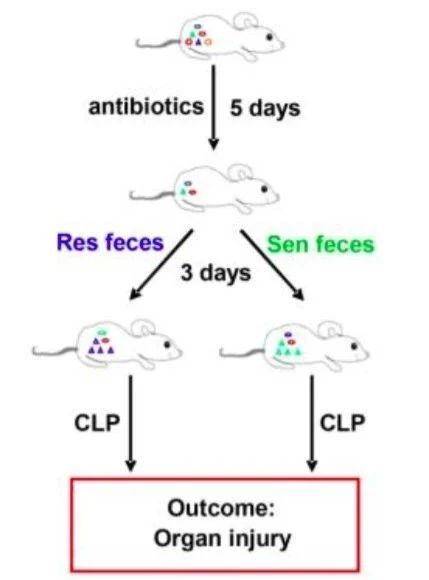
图5 FMT实验流程
该研究表明肠道菌群在脓毒症诱导的肝损伤易感性上发挥了关键调节作用,并确定菌群代谢物GA是在脓毒症的发展过程中是一种新的护肝物质。通过移植非易感性的菌群可以减轻脓毒症导致的肝损伤,粪便肠道菌群移植为脓毒症导致的多器官性功能障碍的治疗提供了新方向。