热搜词:宏基因组测序 芯片检测

发布时间:2020-07-31 15:00:00 点击数:次
近期博越致和客户华中农业大学水产学院刘小玲副教授团队在国际期刊《Frontiers in Immunology》(IF=5.085)上发表题为“Immunomodulatory Effects and Induction of Apoptosis by Different Molecular Weight Chitosan Oligosaccharides in Head Kidney Macrophages From Blunt Snout Bream (Megalobrama amblycephala)”的研究文章。文章中转录组测序技术由武汉博越致和生物科技有限公司提供。

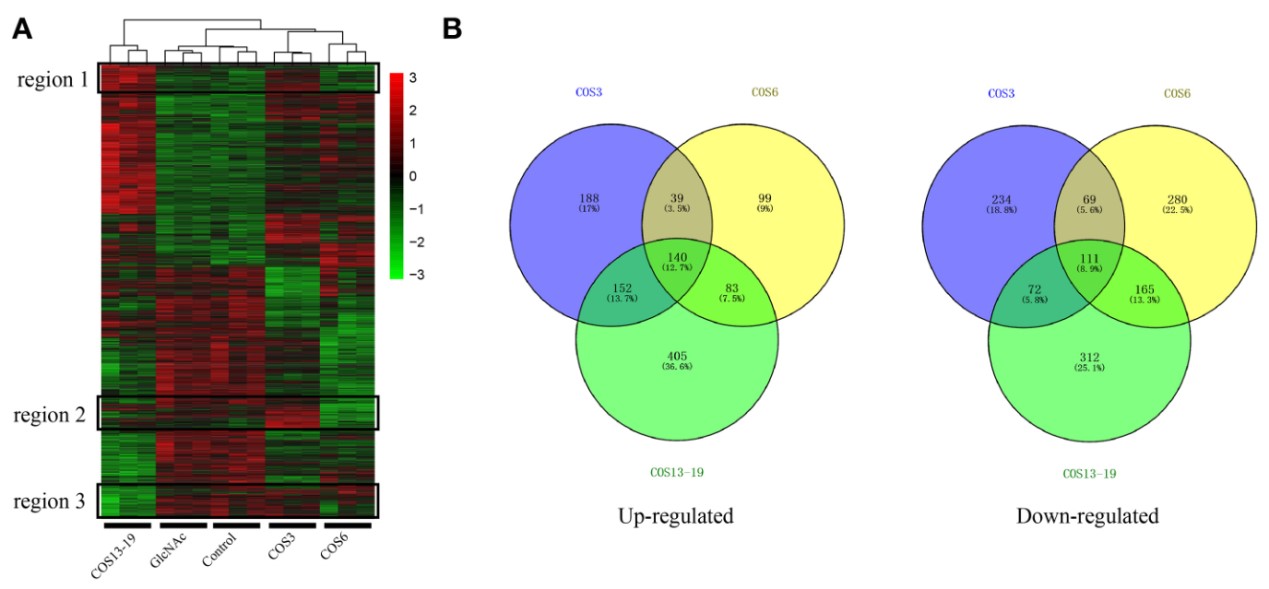
图1 不同MW COS刺激的巨噬细胞的差异表达基因(DEG)分析(P<0.001)
2、DEG的功能富集分析
与对照组相比,COS3,COS6和COS13-19组之间的DEG数量存在明显差异。作者对DEG进行了功能富集(GO)和KEGG通路分析。三组top 15的GO term(按P值的降序排列)如图2所示。三个刺激组中常见的GO term分别是防御反应,炎症反应,对细菌的反应,对生物刺激的反应,对外部生物刺激的反应以及对其他生物的反应(图2A–C)。此外,免疫相关反应在一组或两组中富集到,主要包括免疫系统过程(COS6和COS13-19),免疫系统过程的调节(COS6)和白细胞趋化性(COS13-19)。在KEGG富集的GSEA分析中显示,三组中top 10的KEGG途径(按NES降序排列)(图2D-F)。与病原体感染相关的一些途径被显著富集,包括沙门氏菌感染(COS3和COS13-19),非洲锥虫病(COS3)和疟疾(COS3)。COS13-19组的免疫相关途径丰富,如TNF信号通路和Toll样受体信号通路。值得注意的是,DNA复制是三组中最突出的途径。这可能反映了COS刺激的巨噬细胞的共同特征。
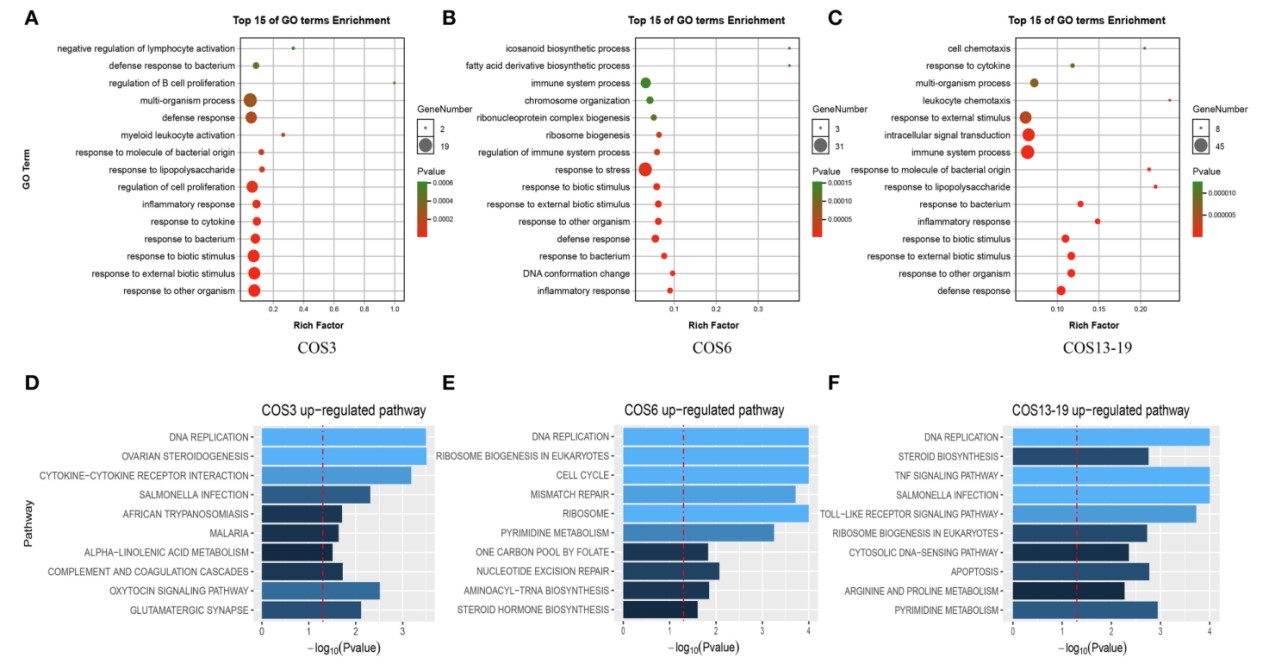
图2 功能富集分析确定了COS3,COS6和COS13-19组中的主要生物学过程和途径
3、COS刺激的巨噬细胞的加权基因网络共表达分析
一个对照组和四个处理组共包含15个样品,在这里使用10,000个基因构建基因共表达网络。14作为允许在五组拓扑模型中获得超过80%相似性的最低值(图3A),共发现了17个重要模块(图3B)。不同模块中包含的基因的数量和百分比如图3C所示。在这些模块中,COS3组中的cyan和magenta模块显着相关,COS6组中的midnight-blue和grey 60模块显着相关,而COS13-19组中的blue模块显著相关(PearsonP>0.8和P<0.001,图3D)。此外,还对5个模块中的GS和MM进行了基因内模分析。由于GS和MM表现出显著的相关性,因此本发现暗示该模块中的基因倾向于与COS刺激的巨噬细胞高度相关,magenta,midnight-blue和blue模块在COS3,COS6和COS13三组中相关性最高,分别为19组(图3E-G)。这可能表明这些基因在三组中有助于巨噬细胞的状态,因此作者选择了三个模块进行进一步分析。
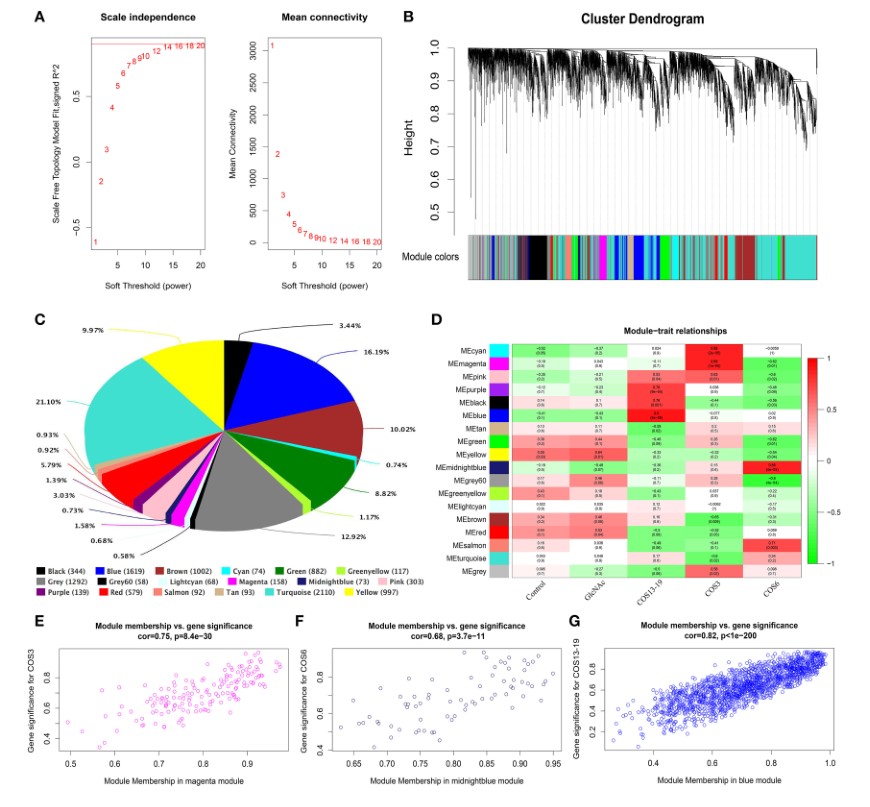
图3 加权基因共表达网络分析(WGCNA)
4、网络建设与部分模块分析
如图4A–C所示,构建了magenta,midnight-blue和blue基因的共表达网络。选择了blue模块中的200个基因来显示基因间连接和确认中心基因。在每个网络中,颜色深度,字体大小和节点大小与它们的连通性(模块内度之和)成正比。为了研究品magenta,midnight-blue和blue模块的生物学功能,作者进行了GO富集分析。magenta模块中显示top 5的GO term(图4D)分别是肽基脯氨酸羟基化,蛋白质羟基化,单一生物代谢过程,mRNA转运和氧化还原处理。另外,在图4A中,已证明EGLN1A,ERO1A,EGLN3,P4HA2和CPOX的中枢基因与细胞内氧浓度有关。EGLN1A催化缺氧诱导因子(HIF)α蛋白中4-羟基脯氨酸的翻译后形成。在midnight-blue模块中,top5的GO term包括补体激活的经典途径,MAPK级联的负调控,蛋白质对染色质的定位,白细胞介导的免疫和磷脂转运(图4E)。该模块中的中枢基因与先天免疫系统和细胞增殖有关,例如DUSP2,C1QB,CFP,SPRY4,C1QC,EMILIN1B,WNK4B,ZFP36L1,EGR3等(图4B)。在blue模块中,富集到细胞内信号转导,MAPK级联,细胞死亡,死亡和程序性细胞死亡GO term(图4F),以及与先天免疫和抗肿瘤活性相关的中枢基因,例如MAP3K12,FMN1,MPX ,ABI3A,SLC2A6,TNFAIP2B,DUSP1,NOS2B,JUN,IL1β等(图4C)。为了进一步探索由COS13-19刺激的巨噬细胞的潜在功能,使用STRING数据库中的有关蛋白质-蛋白质相互作用的现有数据来检查blue模块的生物学特性。作者在PPI网络中选择相互作用评分≥0.4的蛋白质,以进行KEGG途径富集分析以及蛋白质家族和结构域准确分类。图4G中富集到top 10的路径,这些途径与传染病,免疫系统,细胞生长和死亡,信号转导和代谢有关。蛋白质家族和结构域的富集结果包括caspase募集结构域,bZIP转录因子和PH结构域(图4H),这些结果可能暗示COS13-19不仅激活巨噬细胞的免疫系统,而且还调节细胞增殖和通过某些途径(例如FoxO,MAPK和p53信号传导途径和细胞周期)凋亡。总体而言,在已知调节免疫系统,细胞生长和死亡的三个模块中鉴定一些基因以及基因表达网络分析使用WGCNA方法可为调节巨噬细胞的途径提供有价值的见解,而巨噬细胞是由COSs刺激的巨噬细胞所致。
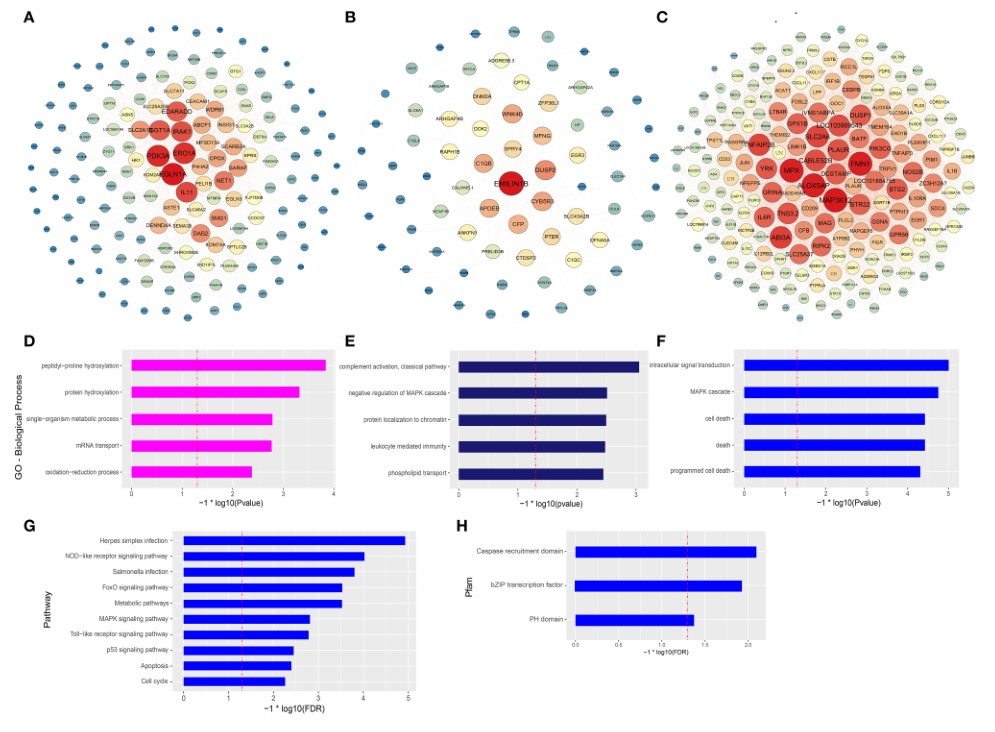
图4 基因网络和所选模块的富集分析
5、钝嘴鼻头肾脏巨噬细胞中COSs激活的MAPK和NF-κB信号通路
在哺乳动物研究中,COS可通过静止的巨噬细胞促进细胞因子的分泌,并在炎症和免疫反应中起重要作用。研究最多的两个通路是MAPK和NF-κB信号通路。MAPK途径和NF-κB上游途径得到了丰富。为了进一步验证结果,作者选择了qwew在不同时间点(4、8和16h)刺激的巨噬细胞和两种途径的关键基因进行qRT-PCR分析。如图5所示,ERK1/2,Jnk1,P38α,P38β,Fos,Junb和Jund是MAPK途径的关键基因(图5A-H)。qRT-PCR结果表明,COS可以在巨噬细胞刺激的早期(4h)通过p38β激活MAPK途径,然后上调其他基因。在NF-κB途径中(图5I-K),在4h时COS6和COS13-19组中NF-κB2显着上调,而NF-κB1和炎性细胞因子TNF-α的表达上调。这些结果再次证明,MAPK和NF-κB信号通路在COS刺激的巨噬细胞中被激活。
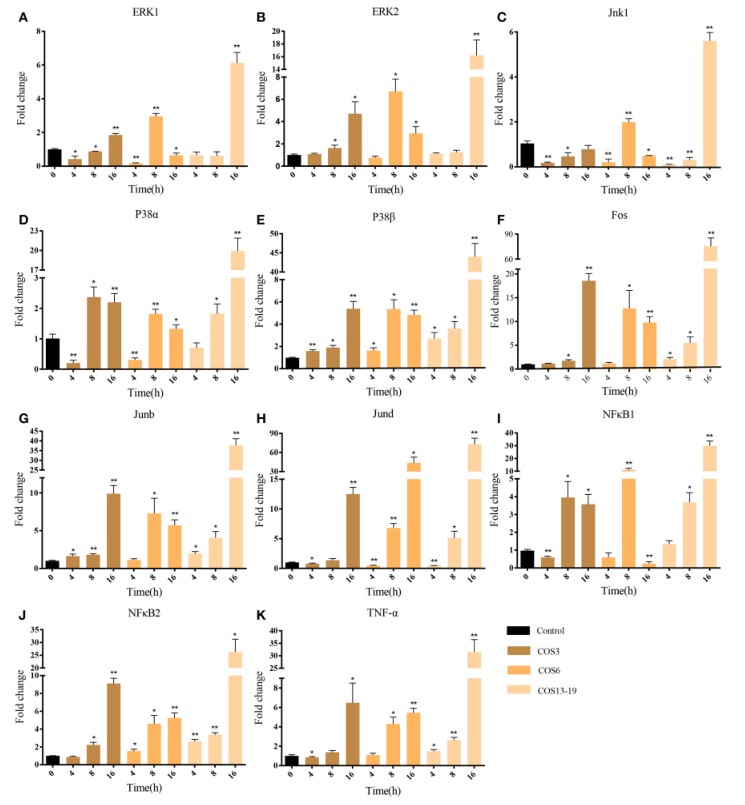
图5 qRT-PCR鉴定了MAPK和NF-κB通路的关键基因表达
6、COS通过P53途径诱导巨噬细胞凋亡
P53激活不仅导致细胞周期停滞,而且参与细胞凋亡,从而导致两个不同的结果:前者为细胞提供了启动修复和逆转损伤的可能性。后者对细胞具有致命性。因此,p53被认为是决定细胞存活和死亡的关键因素之一。在结果中,P53途径,细胞死亡相关的GO term和caspase募集域得到了丰富。为了进一步验证结果,使用了qRT-PCR和免疫荧光染色方法。这些结果如图6所示。在刺激的早期阶段(4h),只有ATR和P53基因被显着上调,而Bax和Caspase 3随后被显着上调(图6A–E)。免疫荧光染色的结果表明在刺激后16h发生凋亡,尤其是在COS13-19组中(图6F和图S3)。这些结果表明COS可以通过p53信号通路促进巨噬细胞凋亡。
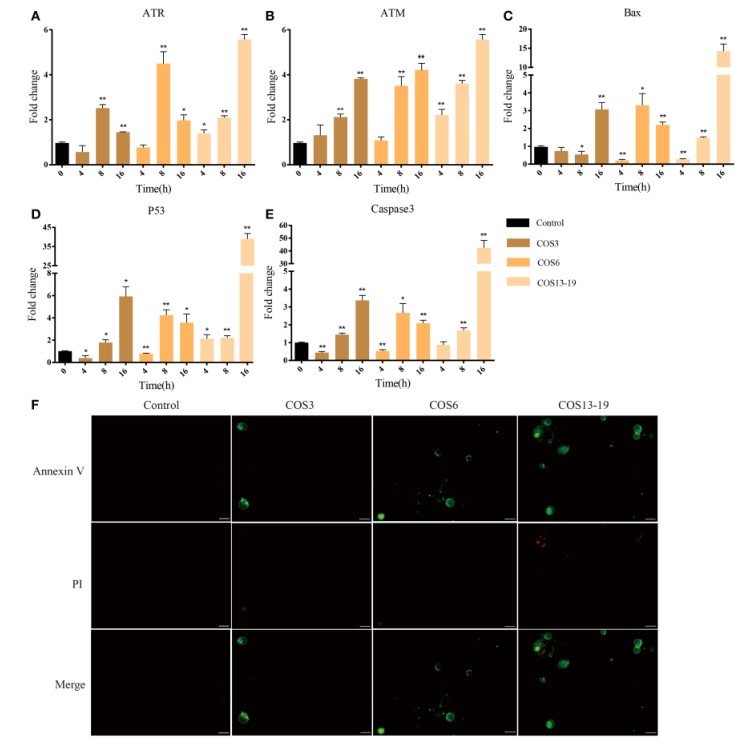
图6 COS通过P53途径体外诱导钝嘴鲷鱼头肾脏巨噬细胞凋亡